Zirconium
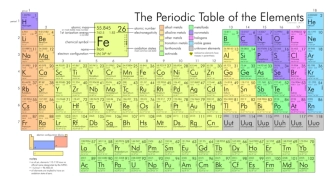
Periodensystem der Elemente
|
Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
Allgemein | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Name, Symbol, Ordnungszahl |
Zirconium, Zr, 40 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Serie |
Übergangsmetalle |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Gruppe, Periode, Block |
4, 5, d |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Aussehen |
silbrig weiß |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
CAS-Nummer |
7440-67-7 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Massenanteil an der Erdhülle |
0,021 % |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Atomar | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Atommasse |
91,224 u |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Atomradius (berechnet) |
155 (206) pm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Kovalenter Radius |
148 pm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Elektronenkonfiguration |
[Kr] 4d2 5s2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
1. Ionisierungsenergie |
640,1 kJ/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
2. Ionisierungsenergie |
1270 kJ/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
3. Ionisierungsenergie |
2218 kJ/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
4. Ionisierungsenergie |
3313 kJ/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Physikalisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Aggregatzustand |
fest |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Modifikationen |
zwei (α-/β-Zr) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Kristallstruktur |
hexagonal; kubisch > 1140 K (867 °C) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Dichte |
6,501 g/cm3 (25 °C) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Mohshärte |
5 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Magnetismus |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Schmelzpunkt |
2130 K (1857 °C) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Siedepunkt |
4650 K (4377 °C) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Molares Volumen |
14,02 · 10−6 m3/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Verdampfungswärme |
591 kJ/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Schmelzwärme |
16,9 kJ/mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Dampfdruck |
0,00168 Pa bei 2125 K |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Schallgeschwindigkeit |
4650 (long.), 2250 (trans.) m/s bei 293,15 K |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Spezifische Wärmekapazität |
270,0 J/(kg · K) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Elektrische Leitfähigkeit |
2,36 · 106 A/(V · m) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Wärmeleitfähigkeit |
22,7 W/(m · K) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Chemisch | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Oxidationszustände |
4, 2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Normalpotential |
−1,553 V (ZrO2 + 4 H+ + 4 e− |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Elektronegativität |
1,33 (Pauling-Skala) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Isotope
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Weitere Isotope siehe Liste der Isotope | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
NMR-Eigenschaften | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
Quelle: Wikipedia, Lizenz für diesen Artikel: Creative Commons Attribution/Share Alike